精彩内容 近日,浙江华义制药以仿制4类报产的米拉贝隆缓释片进入行政审批阶段,获批在即,冲刺首仿。米拉贝隆缓释片是由安斯泰来研发的一款选择性β3-肾上腺素能受体激动剂,2019年全球销售额为1616亿日元,被纳入第二批鼓励仿制目录。 米拉贝隆是由安斯泰
精彩内容
近日,浙江华义制药以仿制4类报产的米拉贝隆缓释片进入行政审批阶段,获批在即,冲刺首仿。米拉贝隆缓释片是由安斯泰来研发的一款选择性β3-肾上腺素能受体激动剂,2019年全球销售额为1616亿日元,被纳入第二批鼓励仿制目录。
米拉贝隆是由安斯泰来研发的一款选择性β3-肾上腺素能受体激动剂,主要用于治疗膀胱过度活动引起的尿急、尿频及尿失禁。该产品最早于2011年9月在日本获批上市,2012年6月在美国获批上市,2017年12月在中国获批上市,2019年全球销售额为1616亿日元(约14.8亿美元)。
显示,2019年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)终端及中国城市实体药店终端米拉贝隆缓释片销售额合计1000万元。该产品在中国公立医疗机构终端的销售额正快速上涨,2019年同比增长3814.29%,2020H1同比增长127.01%。
安斯泰来的米拉贝隆缓释片是国内唯一一款治疗膀胱过度活动症的β3受体激动剂,2020年通过谈判纳入全国医保目录,2021年3月米拉贝隆缓释片正式获纳入第二批鼓励仿制目录。
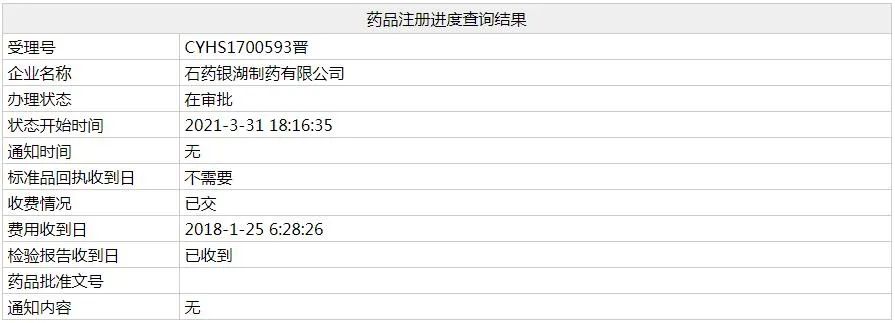
目前国内有3家企业以仿制4类提交米拉贝隆缓释片上市申请,包括浙江华义制药、南京正大天晴、四川国为制药。其中华义制药的产品首家报产,并于2020年3月以“专利到期前1年的药品生产申请”为由纳入优先审评,2021年3月31日该产品注册办理状态变更为“在审批”,若顺利获批将视同过评,拿下首仿。
来源:米内网数据库
注:米内网中国城市实体药店终端竞争格局数据库是覆盖全国293个地市及以上城市实体药店(不含县乡村实体药店),对全品类进行连续监测的放大版城市实体药店数据库。上述销售额以产品在终端的平均零售价计算。
本文来源:米内网 作者:桂枝 免责声明:该文章版权归原作者所有,仅代表作者观点,转载目的在于传递更多信息,并不代表“医药行”认同其观点和对其真实性负责。如涉及作品内容、版权和其他问题,请在30日内与我们联系
 客服微v信:
客服微v信:








 京公网安备 11010802031568号
京公网安备 11010802031568号

